ナノ生命科学研究所/がん進展制御研究所の中山瑞穂准教授,大島正伸教授の研究グループは,腸がん由来オルガノイド(※1)のモデル研究により,悪性化に逆行する細胞集団が,予想以上の頻度で出現していることを発見しました。
がんの悪性化は,遺伝子変異により生存に有利な形質を獲得した腫瘍細胞が,選択的に増殖することで進行すると考えられています。このようながんの悪性化機構は,ダーウィン進化論(※2)に共通する機構として考えられています。しかし,遺伝子変異により悪性化形質を獲得したがん細胞が,その形質を維持し続けるのかについて,いまだ十分な解析が行われていませんでした。
がん研究に広く使われる株化がん細胞は,均一な悪性化細胞が選択されているため,何度継代しても悪性化形質が維持されています。一方で,オルガノイド培養したがん細胞集団では悪性度に関する多様性が維持されており,個々の細胞の悪性化形質を追跡することが可能と考えました。研究グループは,4種類の大腸がんのドライバー遺伝子(※3)変異導入により発生したマウス腸管がんからオルガノイドを樹立して,サブクローニング(※4)および移植実験を行い,遺伝子変異により転移性を獲得したがん細胞集団の約30%の細胞で転移性を失っていることを発見しました。また,転移能を失ったがん細胞は,生体内に近い培養条件での増殖率が顕著に低下しており,次第にがん細胞集団からネガティブな選択により排除される可能性を示しました。
これらの知見は,従来考えられたダーウィン進化に基づくがん悪性化モデルに加えて,ネガティブ選択による新たな悪性化の維持機構の存在を示し,将来的には大腸がん治療薬の開発に活用されることが期待されます。
本研究成果は2022年12月28日(日本時間)に『Cancer Science』誌のオンライン版に掲載されました。
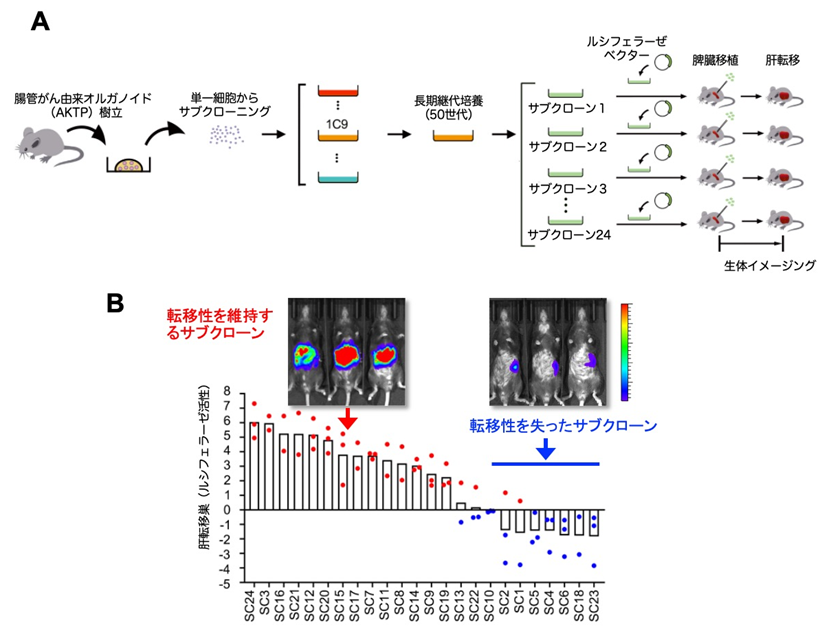
図1
転移性腸がん由来AKTPオルガノイドにおける転移能消失。(A)サブクローニング方法。転移能を獲得した腸管腫瘍からAKTPオルガノイド(1C9)を樹立し,約50世代の長期継代培養の後,単一細胞から24個のサブクローンを作成。(B)各サブクローンを脾臓移植し,ルシフェラーゼによる生体イメージングで肝転移巣を観察すると,約30%で転移性の消失が見られた。
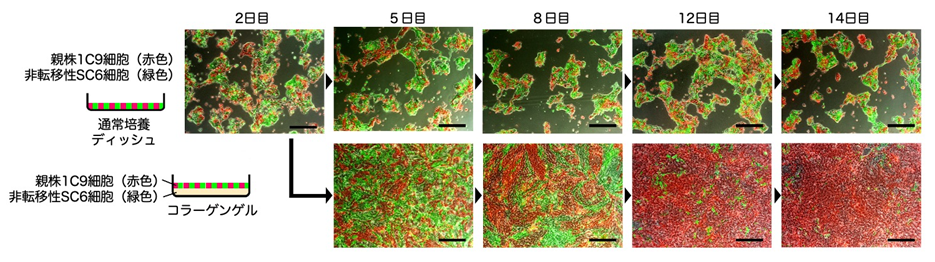
図2
転移性を消失したがん細胞のネガティブ選択による排除。転移性を維持する親株細胞(1C9)を赤色,転移能を失ったサブクローン細胞(SC6)を緑色の蛍光タンパクでそれぞれ標識し,通常培養ディッシュ上で共培養すると双方の細胞集団が均等に増殖を継続するが(上段),コラーゲンゲル上で培養すると,転移能消失細胞は次第に集団から排除される(下段)。
【用語解説】
※1:オルガノイド
正常組織あるいは腫瘍組織由来の上皮細胞を,生体内と同様の多様性を維持したままマトリックス中で3次元培養した組織。生体内の状況に近いと考えられ,培養細胞に代わる方法として広く研究に使われる。
※2:ダーウィン進化論
遺伝子変異により生存に有利な形質を獲得した個体が「自然淘汰」や「適者生存」により選択されて進化するというダーウィンによる進化論。がんの悪性化も,遺伝子変異と選択の繰り返しにより,進展すると考えられている。
※3:ドライバー遺伝子
がん細胞で認められる多数の遺伝子変異の中で,その遺伝子の変異が発がんや悪性化進展に関与する場合,その遺伝子をドライバー遺伝子と呼ぶ。
※4:サブクローニング
細胞集団から単一細胞を取り出し,1細胞からクローナルに増殖させて細胞株を樹立させる手法。サブクローン集団を構成する細胞は,同一の細胞に由来する。
掲載ジャーナル:Cancer Science
研究者情報:大島 正伸




 PAGE TOP
PAGE TOP